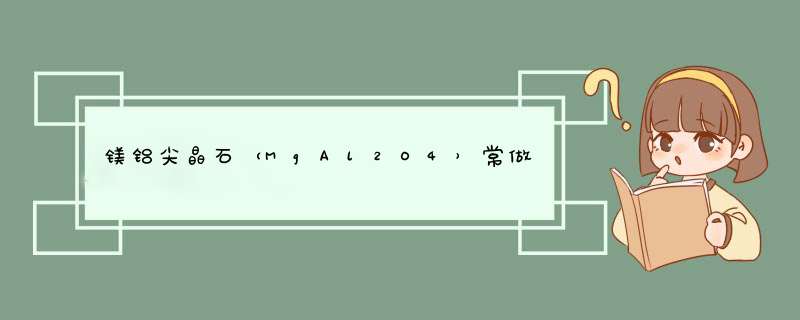
(1)根据微粒电子层越多,半径越大,电子层相同,核电荷数越多,半径越小的规律,离子的半径大小顺序是:Cl->O2->Mg2+>Al3+>H+,
故答案为:Cl->O2->Mg2+>Al3+>H+;
(2)AlCl3与氨水反应生成氢氧化铝沉淀和氯化铵,氯化铵是离子化合物,电子式为:,氢氧化铝是两性氢氧化物,
电离方程式为:H++AlO2-+H2O?Al(OH)3?Al3++3OH-,
故答案为:;H++AlO2-+H2O?Al(OH)3?Al3++3OH-;
(4)a.H2O比NH3稳定,可以证明氧元素的非金属性比氮元素强,故a错误;
b.共用电子对偏向:H-O>H-N,证明氧原子的得电子能力强于氮原子,即氧元素的非金属性比氮元素强,故b错误;
c.沸点:H2O>NH3是物理性质的表现,但是氧元素的非金属性比氮元素强是化学性质的表现,故C正确;
d.NO中氮是+2价,氧是-2价,证明氧原子的得电子能力强于氮原子,即氧元素的非金属性比氮元素强,故d错误;
故选c.
由于镁铝的
热膨胀系数
小,因而以其为结合相的耐火材料
制品
热震稳定性
相对提高。另外,由于尖晶石具有
硬度
大,
化学性能
稳定,
熔点
高等良好的性质,在高温下抵抗各种熔体
侵蚀作用
的能力非常强,所以
在制品
中由于尖晶石
矿体
的存在,改善了制品的高温性能。尽管尖晶石具有上述性质,但天然的镁铝尖晶石却极少,不能满足需要,因此近代一般采用人工
合成法
。
人工合成镁铝尖晶石主要是采用MgO和Al2O3
原料
以电熔法、烧结法或在烧结过程中获得
镁铁尖晶石:含铁的尖晶石。化学式为(Mg, Fe2+ )(Al,Fe3+)2O4,等轴晶系,硬度7.5~8。折射率1.75~1.79,半透明,常呈暗绿、褐、黑等色。
铝镁尖晶石(magnesia-alumina
spinel)是指以氧化镁和三氧化铝为原料,经人工合成的尖晶石质耐火原料。该原料在自然界发现极少,工业用的镁铝尖晶石全是人工合成的。铝矾土基烧结镁铝尖晶石采用Al2O3含量76%以上的优质矾土和MgO含量95%以上的优质轻烧镁粉,经过多级均化工艺,在超高温隧道窑中经1800°C以上高温烧结而成。
欢迎分享,转载请注明来源:夏雨云

 微信扫一扫
微信扫一扫
 支付宝扫一扫
支付宝扫一扫
评论列表(0条)